Chapitres physique-chimie en Première
Exercices corrigés sur les modèles de la lumière en 1ère
Résumé de cours Exercices et corrigés
Cours en ligne de physique-chimie en Première
Ces exercices corrigés au niveau 1ère pour la spécialité physique chimie sur les modèles de la lumière pourront vous aider à mieux comprendre les notions de modèle ondulatoire, modèle particulaire, absorption et émission. Vous pourrez mieux appréhender les exercices sur la découverte du photon et les propriétés radiatives de l’atome d’hydrogène. Si vous avez des difficultés ou souhaitez exceller, nous proposons des professeurs particuliers de physique chimie pour les élèves de première pour travailler à l’aide d’un enseignant de qualité.
Vous pouvez consulter d’autres exercices et corrigés de physique chimie en première sur notre site : Exercice sur le théorème de l’énergie cinétique, exercice et corrigé sur l’énergie mécanique ou encore un exercice sur les ondes mécaniques, etc.
QCM sur les modèles de la lumière en 1ere
Question 1 :
On passe du violet au rouge en multipliant la longueur d’onde par 2.
La fréquence des ondes correspondantes est
a. divisée par 2
b. inchangée
c. multipliée par 2
Question 2 :
Le soleil est à environ 150 millions de km de la Terre.
La lumière émise par le Soleil met environ, pour arriver sur la Terre
a. 2 ms
b. 0,5 s
c. 8 minutes
Question 3 :
Un photon d’énergie ![]() correspond à une onde lumineuse de longueur d’onde
correspond à une onde lumineuse de longueur d’onde
a. ![]()
b. ![]()
c. ![]()
Corrigé du QCM de 1ère sur les modèles de la lumière
Question 1 :
![]()
![]() donc
donc
![]()
Question 2 :
![]()
avec ![]()
donc ![]()
soit environ 8 minutes en divisant par 60.
Question 3 :
![]()
avec ![]()
COURS DE PHYSIQUE-CHIMIE
Nous avons sélectionné pour vous les meilleurs profs particuliers.
POUR ACCÉLÉRER MA PROGRESSION EN PHYSIQUE-CHIMIE, JE TROUVE DES
Avis Google France ★★★★★ 4,9 sur 5
Exercices sur les modèles de la lumière en 1ère
Exercice sur la découverte du photon en 1ère
L’effet photoélectrique peut être décrit ainsi. Une plaque de métal est soumise à un rayonnement lumineux intense. On cherche ainsi à arracher des électrons à cette plaque. Si des électrons sont arrachés, on les accélère et on les récupère sur une électrode appelée anode, on détecte alors un courant électrique. Les faits théoriques et expérimentaux sont les suivants.
(1) Pour arracher un électron, il faut qu’il reçoive une énergie minimale ![]()
(2) Si on éclaire la plaque avec une lumière de longueur d’onde ![]() supérieure à une certaine valeur
supérieure à une certaine valeur ![]() , on ne détecte aucune intensité électrique, et ceci quelle que soit la puissance de l’éclairement.
, on ne détecte aucune intensité électrique, et ceci quelle que soit la puissance de l’éclairement.
(3) Lorsque la longueur d’onde de la lumière est inférieure à ![]() , on détecte une intensité électrique qui augmente lorsqu’on augmente la puissance de l’éclairement.
, on détecte une intensité électrique qui augmente lorsqu’on augmente la puissance de l’éclairement.
a. Expliquer comment ces propriétés permettent de valider le modèle du photon.
b. Pour un métal donné, ![]() et
et ![]()
Calculer la valeur de la constante de Planck.
Exercice sur les propriétés radiatives de l’atome d’hydrogène en première
Voici le diagramme énergétique de l’atome d’hydrogène.
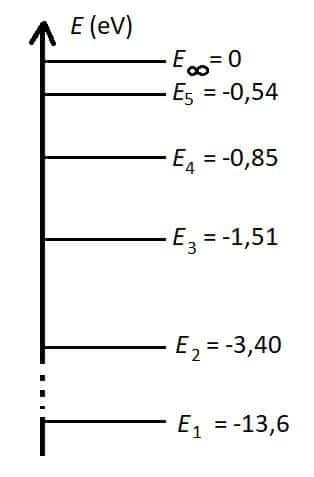
a. Montrer que ce diagramme est compatible avec la formule théorique
![]()
b. Quelle énergie ![]() , exprimée en J, faut-il donner à un atome d’hydrogène dans son état fondamental pour l’ioniser ? Calculer la longueur d’onde
, exprimée en J, faut-il donner à un atome d’hydrogène dans son état fondamental pour l’ioniser ? Calculer la longueur d’onde ![]() et préciser dans quel domaine de radiations elle se trouve.
et préciser dans quel domaine de radiations elle se trouve.
c. Quelle énergie minimale ![]() , exprimée en J, faut-il donner à un atome d’hydrogène dans son état fondamental pour l’exciter ? Calculer la longueur d’onde
, exprimée en J, faut-il donner à un atome d’hydrogène dans son état fondamental pour l’exciter ? Calculer la longueur d’onde ![]() et préciser dans quel domaine de radiations elle se trouve.
et préciser dans quel domaine de radiations elle se trouve.
d. En se limitant aux 5 premiers niveaux d’énergie, combien de raies (dans le visible et dans l’invisible) apparaissent dans le spectre de l’atome d’hydrogène ?
e. La série de Lyman correspond aux transitions ![]() avec
avec ![]() . Justifier que ces raies se trouvent dans l’UV.
. Justifier que ces raies se trouvent dans l’UV.
f. La série de Paschen correspond aux transitions ![]() avec
avec ![]() . Justifier que ces raies se trouvent dans l’IR.
. Justifier que ces raies se trouvent dans l’IR.
g. La série de Balmer correspond aux transitions ![]() avec
avec ![]() . Calculer les deux longueurs d’onde correspondant à
. Calculer les deux longueurs d’onde correspondant à ![]() ,
, ![]() et
et ![]() et indiquer les couleurs correspondant à ces raies.
et indiquer les couleurs correspondant à ces raies.
h. Commenter les spectres suivants, d’émission et d’absorption de H.

i. Voici un extrait du spectre de la lumière venant du Soleil
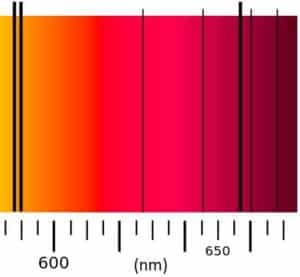
Justifier la présence d’hydrogène dans l’atmosphère qui entoure le Soleil.
COURS PARTICULIERS DE PHYSIQUE
Nous avons recruté pour vous les meilleurs profs de physique.
POUR M'AMÉLIORER EN PHYSIQUE, JE CHERCHE DES
Avis Google France ★★★★★ 4,9 sur 5
Corrigé des exercices sur les modèles de la lumière en 1ere
Corrigé de l’exercice sur la découverte du photon en première
a. Dans un modèle non-particulaire de la lumière, plus la puissance de l’éclairement est grande, plus l’énergie frappant la plaque par seconde serait grande. Lorsque cette énergie rapportée à un atome de la plaque dépasse ![]() , d’après (1), un électron serait arraché et on détecterait une intensité électrique. Ceci est contredit par (2).
, d’après (1), un électron serait arraché et on détecterait une intensité électrique. Ceci est contredit par (2).
Dans le modèle particulaire du photon, l’énergie du photon vaut ![]() . On en déduit que
. On en déduit que ![]() .
.
* Lorsque ![]() ,
, ![]() alors le photon ne peut pas arracher l’électron de l’atome, et ceci quel que soit le nombre de photons apportés par seconde, ce qui est conforme à (2).
alors le photon ne peut pas arracher l’électron de l’atome, et ceci quel que soit le nombre de photons apportés par seconde, ce qui est conforme à (2).
* Lorsque ![]() ,
, ![]() alors le photon peut arracher l’électron de l’atome et on détecte une intensité électrique. Plus la puissance lumineuse est grande, plus le nombre de photons frappant la plaque par seconde est grand, donc plus le nombre d’électrons arrachés par seconde est grand, donc plus l’intensité lumineuse est grande, ce qui est conforme à (3).
alors le photon peut arracher l’électron de l’atome et on détecte une intensité électrique. Plus la puissance lumineuse est grande, plus le nombre de photons frappant la plaque par seconde est grand, donc plus le nombre d’électrons arrachés par seconde est grand, donc plus l’intensité lumineuse est grande, ce qui est conforme à (3).
b. On convertit
![]()
On peut écrire
![]()
Corrigé sur les propriétés radiatives de l’atome d’hydrogène
a. On calcule les énergies pour ![]() = 1, 2, 3, 4, 5 et on vérifie qu’on obtient bien les valeurs indiquées dans le tableau.
= 1, 2, 3, 4, 5 et on vérifie qu’on obtient bien les valeurs indiquées dans le tableau.
Par exemple pour ![]()
![]()
b. L’ionisation correspond à la transition ![]()
Il faut donc donner une énergie
![]()
On en déduit
![]()
qui est dans le domaine UV.
c. La plus petite transition possible est ![]()
Il faut donc donner une énergie
![]()
On en déduit
![]()
qui est dans le domaine UV.
d. En notant ![]() la transition
la transition ![]() , les transitions possibles pour l’émission d’un photon (
, les transitions possibles pour l’émission d’un photon (![]() ) sont
) sont
(51) (41) (31) (21)
(52) (42) (32)
(53) (43)
(54)
soient 10 raies.
e. La plus petite transition est ![]() , la longueur d’onde correspondante est la même que celle calculée à la question c (réciprocité) et vaut 124 nm, dans le domaine UV.
, la longueur d’onde correspondante est la même que celle calculée à la question c (réciprocité) et vaut 124 nm, dans le domaine UV.
Toutes les autres transitions produisent un photon d’énergie plus grande, donc de longueur d’onde plus petite, et sont donc dans l’UV
f. Toutes les transitions produisent un photon d’énergie inférieure à
![]()
donc de longueur d’onde supérieure à
![]() qui est dans le domaine de l’IR.
qui est dans le domaine de l’IR.
g. ![]() (rouge)
(rouge)
![]() (bleu)
(bleu)
![]() (violet)
(violet)
h. On observe parfaitement la complémentarité des spectres (un photon ne peut être émis que s’il peut être absorbé).
On identifie bien les trois raies de la série de Balmer calculées à la question g. La quatrième, plus loin dans le violet, correspond certainement à la transition ![]() .
.
i. On identifie la raie noire d’absorption dans le rouge au voisinage de 658 nm (la valeur exacte est 656,281) qui est la signature de la présence de l’hydrogène.
Retrouvez d’autres cours en ligne gratuits en 1ère sur notre site :

